ARCANE
Alexandre Bourles

L'émergence et la propagation rapides de bactéries pathogènes (multi)résistantes aux antimicrobiens est un enjeu de santé prioritaire au niveau mondial. Malgré son insularité, la Nouvelle-Calédonie n'a pas été préservée de cette pandémie et la résistance aux antibiotiques représente un enjeu de santé publique majeur sur le territoire. Les travaux menés sur le territoire sont axés sur des approches cliniques et il n’existe pas à ce jour d’étude portant sur le rôle de l'environnement dans la sélection et la dissémination de bactéries résistantes aux antibiotiques.
Dans ce sens, le projet ARCANE propose d’étudier la résistance des populations bactériennes dans les eaux usées (d’origine hospitalière ou de la population générale) et l'environnement récepteur (eau de mer côtière).
Du point de vue de la santé publique ce projet permettra de dresser un état des lieux de l’antibiorésistance dans l’environnement néo-calédonien et d’identifier des points critiques susceptibles d’être la cible d’actions de contrôle visant à limiter la propagation de la résistance aux antimicrobiens.
Durée de projet 19 mois
Programme associé

Responsable scientifique
Pôle Bactériologie – Unité de Bactériologie Expérimentale
L'émergence et la propagation rapides de bactéries pathogènes (multi)résistantes aux antimicrobiens est un enjeu de santé prioritaire au niveau mondial. Malgré son insularité, la Nouvelle-Calédonie n'a pas été préservée de cette pandémie : le territoire a ainsi été le pays hôte du premier isolat français porteur du gène plasmidique mcr-1 (conférant une résistance à la colistine). D'autres résistances sont de plus en plus préoccupantes car elles entraînent des problèmes de santé publique importants sur le territoire. A titre d'exemple, le Staphylococcus aureus résistant à la méthicilline diffuse au sein de la population avec des souches à haute virulence et les Entérobactéries Productrices de Carbapénémases (EPC) sont impliquées dans des épidémies au sein du Centre Hospitalier Territorial.
La sélection et la transmission de ces résistances sont fréquemment investiguées via des études cliniques et ce n'est que récemment que le rôle de l'environnement comme source et voie de diffusion de la résistance aux antibiotiques a été reconnu. En effet, les effluents des hôpitaux, de l'industrie, des structures d’élevage ou vétérinaires, des stations d’épuration et des eaux de ruissellement urbaines/agricoles sont autant de sources potentielles de nouveaux contaminants (antibiotiques, biocides, métaux, gènes de résistance, bactéries résistantes) pouvant se déverser dans les milieux récepteurs. Au-delà des apports anthropiques, les fortes concentrations en métaux retrouvées naturellement peuvent constituer des facteurs favorables à l’émergence et/ou la sélection de bactéries résistantes aux antibiotiques. En effet, les gènes de résistance aux métaux et aux antibiotiques peuvent être situés sur les mêmes éléments génétiques mobiles (co-resistance), ou un mécanisme identique peut être impliqué dans la résistance aux antibiotiques et aux métaux (cross-resistance).
Parmi les techniques visant à mettre en évidence ces sources de contaminants et les risques pour la santé humaine, l'épidémiologie basée sur l’analyse des eaux usées via des approches métagénomiques s’est développée ces dernières années. Ces approches innovantes permettent d’identifier les espèces bactériennes mais aussi de quantifier et décrire des milliers de gènes (ex. de résistance ou de virulence) dans un échantillon donné.
En Nouvelle-Calédonie, à ce jour, aucune étude visant à identifier des bactéries résistantes dans les eaux usées, les eaux de ruissellement ou le milieu récepteur n’a été menée. Il existe pourtant un besoin réel sur le territoire puisque, lors de fortes pluies par exemple, il n’est pas rare d’assister à des phénomènes de contaminations bactériennes des zones de baignade. Le suivi sanitaire des eaux de baignade est réalisé annuellement pendant la période estivale (de décembre à avril) par la Direction des Affaires Sanitaires et Sociales du gouvernement de la Nouvelle-Calédonie sur l’ensemble du territoire. Dans certaines communes, des analyses complémentaires et réglementaires sont également réalisées. Ces suivis portent sur le dénombrement des Escherichia coli et des entérocoques intestinaux sans information sur le niveau de résistance aux antibiotiques de ces souches, pourtant reconnues comme étant potentiellement porteuses de résistances.
Dans ce contexte, les objectifs du projet ARCANE sont d’évaluer la dissémination des gènes de résistance et des bactéries résistantes aux antibiotiques dans l’environnement, via une approche intégrée environnementale innovante. Grâce au développement d’une technologie novatrice de suivi des concentrations en métaux et en antibiotiques, ce projet permettra également d’identifier de possibles facteurs d’origine anthropique ou environnementale susceptibles de favoriser la sélection, le développement et la dissémination de souches résistantes.
Ce projet regroupe trois partenaires du CRESICA : l’Institut Pasteur de Nouvelle-Calédonie (IPNC), le Centre Hospitalier Territorial (CHT) via les laboratoires de bactériologie,d’Hygiène et Environnement et de Toxicologie, et l’Institut de Recherche pour le Développement (IRD) via le Laboratoire des Moyens Analytiques (LAMA). La partie métagénomique sera réalisée en partenariat avec l’Institut Pasteur à Paris (IPP) et les dosages des métaux et des antibiotiques impliqueront le laboratoire AEL. Ce projet associe également les collectivités et insitutions de la Nouvelle-Calédonie compétentes au niveau sanitaires (DASS, DAVAR, Mairie de Nouméa, Mairie de Dumbéa, SIVOM-VKP), ainsi qu’au niveau de l’Environnement (Province Sud et Province Nord) pour les différents sites échantillonnés, les établissements de soins concernés par l’étude (CHT, PSN) ainsi que les gestionnaires des systèmes d’épurations retenus (CDE et Epureau).
Du point de vue « Une seule Santé », cette approche intégrée de l’antibiorésistance permettra d’identifier des points critiques susceptibles d’être la cible d’actions de contrôle visant à limiter la propagation de la résistance aux antibiotiques. Sur le long terme, cette approche via l’analyse des eaux usées, pourrait être utilisée dans le suivi au long cours de l’évolution de l’antibiorésistance et comme mesure de l’impact des mesures correctives mises en place.

-
Échantillonnage
Le suivi sera réalisé de façon longitudinale lors d’une campagne de prélèvements sur 14 mois (Prélè
vements tous les deux mois). Les sites d’échantillonnages ciblés suivent le parcours des eaux usées : des effluents des structures de soins jusqu’au milieu récepteur en passant par les structures mises en place pour l’assainissement. Des prélèvements ponctuels d’eau ainsi que des bilans 24h seront réalisés sur certains sites pour avoir un échantillon représentatif.
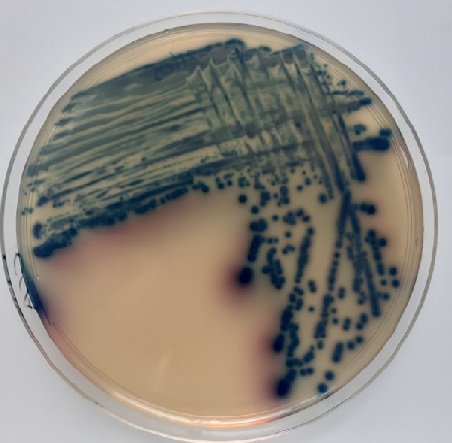
2. Culture
Concernant les isolements, une sélection d’isolats environnementaux, avec un focus plus particulier sur les Entérobactéries Productrices (i) de carbapénémases, (ii) de béta-lactamases à spectre étendu et (iii) de céphalosporinases de hauts niveaux est réalisé. La technique repose sur l’ensemencement directement sur un milieu de culture ou la filtration d’échantillons d’eau et le dépôt des membranes sur des géloses sélectives permettant d’isoler des entérobactéries résistantes aux β-lactamines. Une identification par MALDI-ToF est réalisée et des tests de synergie permettent d’identifier le mécanisme de résistance impliqué. Les isolements permettent d’obtenir une vue d’ensemble du panel de résistance retrouvé au sein des bactéries cultivables dans l’environnement en Nouvelle-Calédonie. En fonction des résultats, un certain nombre d’isolats sera soumis à un séquençage du génome complet qui permettra d’identifier les gènes et les éléments génétiques mobiles impliqués dans la résistance et qui servira de référence pour les analyses en métagénomique. En parallèle, des génomes complets d’isolats cliniques et de l’environnement hospitalier d’intérêt alimenteront la base de données.
3. Métagénomique
Pour la métagénomique, la technique proposée consiste à recueillir les organismes et débris d’organismes présents dans l’eau par filtration à 0,22 µm. L’ADN sera extrait puis un séquençage de type Shot Gun sera réalisé. Cette approche permet d’avoir un aperçu global de la composition du microbiome ainsi que son potentiel fonctionnel par l’identification des gènes et des éléments génétiques mobiles représentés. Les séquences consensus obtenues après assemblage des lectures issues du séquençage seront alignées sur des génomes référencés pour l’identification des espèces formant le microbiome. Des comparaisons des communautés bactériennes échantillonnées dans les différents environnements ainsi que des profils de résistance et leurs variations dans le temps et l'espace seront réalisées. L’approche longitudinale de la source aux eaux littorales permettra de décrire finement les transferts de germes et de gènes de résistance et de documenter les risques sanitaires.
4. Suivi intégrateur des métaux et des antibiotiques
Une technique intégratrice pour l’analyse des éléments traces métalliques et des antibiotiques à l’état de traces et ultra-trace sur résine en couche mince (Diffusive Gradient in Thin film ; DGT) sera utilisée en supplément de dosages classiques sur des eaux.
Les 28 et 29 mars 2022, le CRESICA organisait le séminaire "Au fil de l'eau" qui a permis de présenter l'état d'avancement du projet.
Visionnez la présentation fait lors du séminaire grâce à la vidéo du projet du projet ARCANE par A. Bourles.
Le 29 août 2023, le CRESICA organisait le séminaire de restitution "Au fil de l'eau" qui a permis de présenter les résultats du projet.
Brochure : "Des projets de recherche sur la thématique de l'eau en Nouvelle-Calédonie."
Visionnez la présentation faite lors du séminaire grâce à la vidéo du projet ARCANE par A.Bourles
Rapport final : projet ARCANE